Исследование Йельского университета раскрывает потенциальную причину болезни Альцгеймера
В течение десятилетий
преобладающая гипотеза о причине
появления болезни Альцгеймера, вращалась вокруг амилоидных бляшек
— запутанных скоплений белка бета-амилоида. Их накопление в мозгу пациентов с
деменцией постоянно наблюдается с тех пор, как Алоис Альцгеймер впервые изучил
ее более века назад.
И ученые
сосредоточили бы большую часть исследований на уменьшении и удалении этих
бляшек, но, к сожалению, ряд лекарств постоянно терпел неудачу в клинических
испытаниях. Хотя бляшки явно каким-то образом связаны с болезнью, либо сами по
себе они являются симптомом, либо их удаляют слишком поздно, чтобы устранить
причиненный ими ущерб.
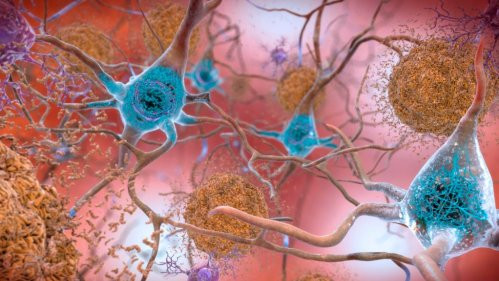
В новом
исследовании ученые из Йельского университета обратили внимание на другую
особенность, которая обычно появляется при болезни Альцгеймера — небольшие
сфероидальные опухоли. Они образуют около амилоидных бляшек вдоль аксонов - длинных,
цилиндрических отростков нейронов, которые позволяют им посылать сигналы другим
нейронам. Как ни странно, любая потенциальная роль, которую они могут играть в
патологии болезни, ранее подробно не изучалась.
Исследователи
обнаружили, что они могут ослаблять передачу электрических сигналов по аксонам.
Чем больше опухоль, тем больше нарушение сигналов, что может способствовать
неврологической дегенерации, наблюдаемой при деменции.
«Мы
идентифицировали потенциальную сигнатуру болезни Альцгеймера, которая имеет
функциональные последствия для схем мозга, при этом каждый сфероид может
нарушить активность сотен нейронных аксонов и тысяч взаимосвязанных нейронов»,
— сказал доктор Хайме Груцендлер, старший автор исследования.
Команда также определила основную причину появления сфероидов. Лизосомы представляют собой небольшие структуры, которые выполняют функцию утилизации отходов в клетках, но у пациентов с деменцией более высокие уровни белка PLD3, что заставляет лизосомы слипаться внутри аксонов. В конечном итоге это вызывает отек.
В тестах
исследователи использовали генную терапию для удаления PLD3 в нейронах мышиных моделей болезни Альцгеймера.
И действительно, отек аксонов резко уменьшился, что улучшило их электрическую
проводимость, а также функцию нейронов в этой области мозга.
Исследователи
говорят, что PLD3 может стать
биомаркером болезни Альцгеймера, позволяя диагностировать ее раньше и стать
новой мишенью для потенциальных методов лечения.
«Возможно,
удастся устранить нарушение электрических сигналов в аксонах, нацелившись на PLD3 или другие молекулы, которые регулируют
лизосомы, независимо от наличия бляшек», — сказал Груцендлер.
Конечно, есть
некоторые предостережения. Пока исследования проводились только на мышах,
поэтому до применения на людях еще далеко. Кроме того, существуют
противоречивые исследования роли, которую PLD3 играет в развитии болезни Альцгеймера, указывая
на то, что она довольно сложна и может быть не такой простой.
Исследование
опубликовано в журнале Nature.
Комментарии: